

疗效不佳,全球首个体内基因编辑疗法按下暂停键
source link: https://www.36kr.com/p/2011354812360067
Go to the source link to view the article. You can view the picture content, updated content and better typesetting reading experience. If the link is broken, please click the button below to view the snapshot at that time.
即便是最伟大的造物主,工作也有出错的时候。体现在人类身上,造物主无意间搞错的一个基因,就可能给一个人带来终生的疾病折磨。
好的一点是,人类向来有逆天改命的野心。一直以来,医学界都在试图通过后天的努力,去弥补造物主的疏忽。基于此,基因编辑工具不断迭代。
CRISPR技术的诞生,让基因编辑从直板机步入智能机时代,也让我们距离成功修补人类基因缺陷的目标越来越近。
如今,医学界诸多大咖,就在基于CRISPR技术尝试对人体基因组特定目标基因,进行修饰、改造,且从体外编辑到体内编辑,步子越迈越大。
不过,从理想到现实,总有鸿沟需要逾越。
现实中,即便是背靠超级大咖的明星公司Editas,在新技术的研发上,也不一定能总是成功。
11月17日,Editas公司宣布,暂停全球首个体内基因编辑疗法EBT-101的临床研究。背后原因,或许是由于EBT-101的疗效不及预期。
当日,受这一消息影响,这家明星公司股价大跌10.12%,市值仅剩7.5亿美元,较巅峰时期的市值(68亿美元)缩水近90%。
巨大的落差也在告诉我们,不管是大咖还是“黑科技”,都难以让创新药研发一步难登天。
01 被寄予厚望的体内基因编辑疗法
理论上,CRISPR基因疗法可以改变基因、修复基因、筛选基因,帮助人类改变DNA和RNA。说句夸大的话,未来在CRISPR基因疗法的支持下,人类可以成为自己的造物主。
当然,这一目标的实现可能还需要很久。当前,CRISPR基因疗法的使用场景还是集中于单基因遗传病。根据是否在体内编辑,又可以大体分为两类:
一类是体外基因编辑疗法,通过提取患者的病变细胞在体外进行基因编辑,之后再将细胞回输;
另一类是体内基因编辑疗法,通过载体直接将基因编辑系统输送到患者体内,在体内对患者的基因进行修改。
相比之下,体外基因编辑疗法技术更为简单,但制备成本更加高昂;体内基因编辑疗治难度更高,但更具性价比和想象空间。
这是因为,体外基因编辑疗法适用于器官、组织或细胞类型较少,所以大部分适应症集中在血液疾病上;而体内基因编辑疗法则可以用于多种疾病,想象空间更大。
今天我们要说的这家药企Editas ,便是体内基因编辑疗法的先驱。
2013年11月成立的Editas,在问世之初就有多重光环加身。其创始人有手握CRISPR基因编辑专利的生物学家张锋等。
除了金光灿灿的背景之外,Editas公司的药物研发的进展也不慢。
2019年7月25日,Editas公司启动CRISPR/Cas9体内基因编辑疗法EDIT-101的临床试验,旨在纠正视网膜感光细胞的遗传缺陷,以治疗Leber先天性黑蒙10 (LCA10) ,这也是全球首个进入临床的体内基因编辑疗法。
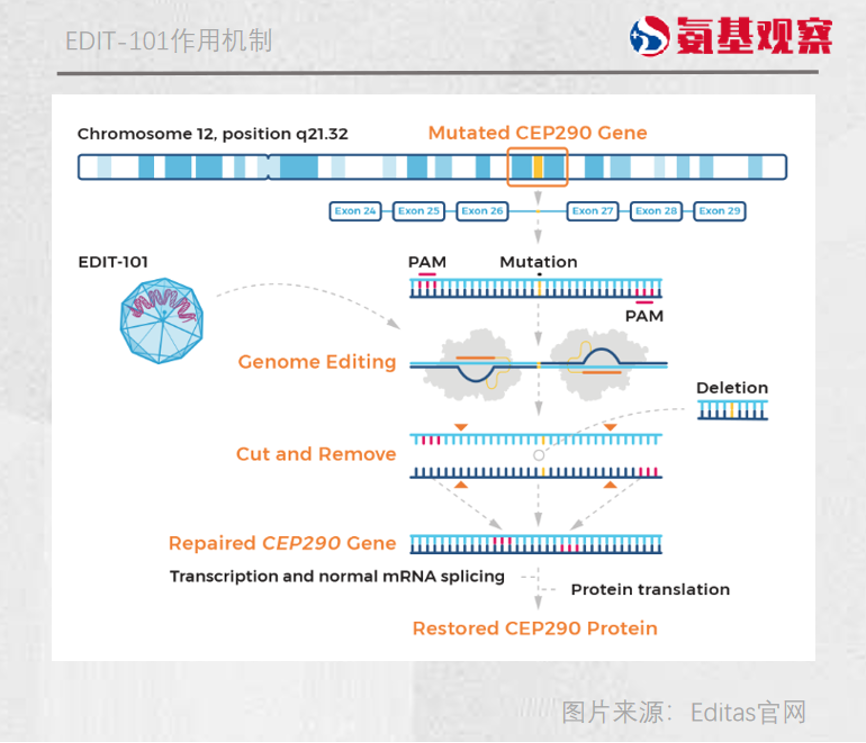
领先的管线,众多大咖的加盟,投资人对Editas的未来充满期待。在2021年1月,虽然尚未有产品问世,但Editas 公司的市值一度冲上了68亿美元。
不过,即便拥有多重光环的加持,Editas的首款体内注射CRISPR/Cas9基因编辑疗法还是暂时翻车了。
02 EDIT-101被按下暂停键
此前,人们对于CRISPR/Cas9体内基因编辑最大的担忧在于安全问题。
核心原因在于,CRISPR-Cas容易“脱靶”,改变其他正常的基因。毫无疑问,这种错误会给患者健康带来新的隐患。
体外基因治疗药物,研发人员可以通过特定的技术,识别脱靶细胞与正常细胞;而在体内,显然很难做到这一点。所以,体内基因编辑的安全问题比体内基因编辑更难掌控。
不过,在前期的临床试验中,EDIT-101似乎不存在安全性问题。
根据EDIT-101早期临床结果,患者在治疗过程只出现了轻中度的治疗相关的炎症,且都可以用类固醇控制。
不过,一款治疗药物除了安全之外,最根本的评价维度还在于效果。
遗憾的是,在疗效的考验上Editas表现的不如人意,其在11月17日公布了EDIT-101的 Ⅰ/Ⅱ期临床试验数据。
这项临床试验招募了14名患者,仅有三名患者对EDIT-101治疗出现反应。并且,其中2名纯合子患者都有反应,但在12个杂合子患者中只有1位患者出现反应。
这也就意味着,EDIT-101对杂合子LCA10患者效果一般,而对纯合子的LCA10患者效果要稍好一些。但要知道,LCA10患者人数本就不多,在美国大约有1500位患者。
而如果将这个范围缩小到纯合子LCA10,患者人数更少,预计仅有300人。先不说EDIT-101目前展现出的效果一般能不能临床成功的问题。
退一步来说,即便Editas公司烧掉所有的钱财,将EDIT-101成功送上市,如此狭窄的患者群体也决定了EDIT-101不太可能有太大的想象空间。
也正是基于这个原因,11月17日,Editas公司宣布暂停EDIT-101的临床试验,寻求合作伙伴继续开发EDIT-101。
作为体内基因疗法的先驱,EDIT-101被按下了暂停键。
03 创新药研发难以一步难登天
EDIT-101的失利,并不意味着体内编辑疗法一定会停止前进,但能够再次告诉我们,创新药研发难以一步登天。
科学技术的发展向来是螺旋式上升的,新技术、新产品从来不会凭空出现。在生物制药领域,这一结论仍然适用。
事实上,生物制药向来是一个需要不断累积经验的领域。其中大部分的新兴技术的成长过程都不会太容易,也不会太短暂。
即便是如今看起来已经成熟的ADC、双抗等技术,在其历史上往回翻几页,也都有过艰苦卓绝的奋斗史。
失败,是创新药,尤其是First in class药物研发的常态。Editas公司的跌倒,对于国内医药市场来说,未尝不是一个启示。
在过去,国内过去并没有真正意义上的First in class药物,大部分药企做的都是风险较低的me too以及fast follow药物,所以很难真正感受到First in class药物研发的残酷性。
如今,随着反对me too的声音变多,使得不少人产生了First in class崇拜,越来越多的创新药玩家开始试水First in class。
不过,在药企踏入这一领域之前,或许要提前做好心理准备。真正九死一生的战争,在这里才刚刚开始。
本文来自微信公众号“氨基观察”(ID:anjiguancha),作者:方涛之,36氪经授权发布。
该文观点仅代表作者本人,36氪平台仅提供信息存储空间服务。
Recommend
About Joyk
Aggregate valuable and interesting links.
Joyk means Joy of geeK